
Abstrak
Penelitian ini menyelidiki biosintesis etil oleat (EO), konstituen utama biodiesel, melalui esterifikasi asam oleat dengan etanol, dikatalisis oleh Candida antarctica lipase B (CALB) yang diimobilisasi pada dukungan berbiaya rendah yang berasal dari lignin ampas apel mete (CAB). Ekstraksi lignin ampas apel mete dilakukan melalui proses asam-basa dan digunakan untuk menghasilkan komposit CAB-lignin terkonjugasi dengan magnetit (Lig-MNP), yang berfungsi sebagai dukungan untuk imobilisasi enzim. Biokatalis (Lig-MNP/CALB), yang diperoleh melalui proses imobilisasi, menunjukkan aktivitas 13 U g −1 dan kemudian diterapkan dalam reaksi esterifikasi untuk mengevaluasi efisiensi katalitiknya dibandingkan dengan enzim bebas. Rasio molar asam terhadap alkohol, suhu, dan beban katalitik dievaluasi. Dalam kondisi optimal – beban katalis 40 mg mL −1 , 40 °C, dan rasio molar 1:2 – Lig-MNP/CALB mencapai konversi EO maksimum sebesar 90%. Enzim yang diimobilisasi menunjukkan stabilitas operasional selama beberapa siklus dan mudah dipulihkan melalui pemisahan magnetik. Biofuel yang dimurnikan mencapai sekitar 90% kemurnian dalam etil oleat dan 98% dalam kandungan ester total. Hasil ini menyoroti potensi biokatalis untuk produksi biofuel berkelanjutan.
Perkenalan
Perubahan iklim merupakan salah satu tantangan paling signifikan bagi umat manusia saat ini dan masa depan. Aktivitas manusia telah meningkatkan CO2 atmosfer hingga 50% sejak akhir abad ke-19, sehingga suhu pada tahun 2023 menjadi 1,36 °C lebih tinggi. 1 Akibatnya, permukaan laut rata-rata global telah meningkat 84,2 mm sejak tahun 1992, dan peningkatan suhu telah memecahkan rekor setiap tahunnya. 2 Skenario ini disebabkan oleh penggunaan bahan bakar fosil dan turunannya, seperti solar, yang mencemari atmosfer dan tanah/air sejak ekstraksi hingga konsumsi.
Sektor transportasi merupakan konsumen energi utama. Diesel merupakan bahan bakar kedua yang paling umum digunakan 3 dan terkenal karena emisi CO 2 dan nitrogen oksida (NO x ), yang berkontribusi terhadap penurunan kualitas udara dan pemanasan global. 4 Di sisi lain, biodiesel merupakan biofuel berbasis karbon dengan lebih sedikit hidrokarbon yang tidak terbakar, tidak mengandung sulfur, tidak mengandung aromatik, dan emisi NOx yang lebih rendah karena kandungan setananya yang tinggi. 5
Etil oleat (EO) merupakan etil ester rantai panjang yang telah banyak diteliti. Etil oleat digunakan dalam berbagai aktivitas industri, termasuk modifikasi lipid, pengolahan minyak omega-3, sebagai pelarut, plasticizer, pelumas, dan biodiesel. 6 Etil oleat juga dapat diproduksi menggunakan asam oleat dan etanol melalui reaksi esterifikasi antara menggunakan Candida antarctica lipase B (CALB) sebagai biokatalis. 7
Salah satu cara untuk meningkatkan penggunaan teknis-ekonomis reaksi esterifikasi enzimatik adalah dengan menggunakan enzim yang diimobilisasi. Namun, prosedur ini dapat memakan waktu dan biaya yang mahal, terutama pada tahap pemurnian. 8 Beberapa pendukung yang secara tradisional digunakan untuk mengimobilisasi enzim, seperti kitosan (€ 2,24/g), karbon nanotube (€ 33,9/g), dan kaca porositas terkontrol (R$ 1820/g), mahal. 9 Bahan berbasis lignin adalah contoh pendukung alami yang mudah ditangani. Misalnya ampas apel mete (CAB) (€ 0,04/kg), yang dikonjugasikan dengan nanopartikel magnetik sebagai pendukung, dapat diterapkan dalam produksi biopelumas 10 dan ester terpena. 11 Menurut Basis Data Statistik Organisasi Pangan dan Pertanian (FAOSTAT, 2025), 12 produksi jambu mete global sekitar 1.328.462,96 ton, dengan Brasil menyumbang 81,2% dari total tersebut. Ampas tebu yang dihasilkan saat ini kurang dimanfaatkan dan sering kali diolah sebagai limbah oleh agroindustri. 11 Pemanfaatannya untuk ekstraksi lignin, dengan senyawa ini selanjutnya digunakan sebagai bahan pendukung, dapat berkontribusi pada pengurangan biaya dan keberlanjutan lingkungan.
Lignin merupakan biopolimer yang menunjukkan kekuatan mekanis, yang penting untuk menjaga integritas struktural enzim yang diimobilisasi 13 dan menahan perubahan suhu dan pH, yang meningkatkan stabilitas enzim dalam reaksi. 14 Lignin juga merupakan material biokompatibel yang memungkinkan pengikatan enzim yang efektif melalui gugus hidroksil yang tersedia dalam strukturnya 15 dan menunjukkan penggunaan ulang yang signifikan, mempertahankan tingkat aktivitas yang tinggi. 16 Properti tersebut penting bagi biokatalis, terutama ketika medan magnet meningkatkan karakteristik kemudahan penanganan dan penggunaan ulangnya.
Penelitian ini menyelidiki produksi etil ester menggunakan lipase B dari CALB yang diimobilisasi ke nanokomposit lignin-magnetit ampas apel mete. Esterifikasi asam oleat enzimatik dilakukan menggunakan etanol dalam pelarut bebas medium, mengevaluasi rasio molar asam:alkohol, suhu, dan beban katalitik. Biodiesel yang diproduksi dalam kondisi sintesis terbaik dimurnikan dan dikarakterisasi.
Bahan dan metode
Bahan
Ampas jambu mete ( Anacardium occidentale L.) dibeli dari koperasi di Pacaju, Ceará, Brasil. Ekstrak enzim lipase B Candida antarctica dibeli dari Sigma-Aldrich (St Louis, AS), dan mengandung 8,5 mg mL −1 protein dengan aktivitas enzimatik 164 U mL −1 . Standar analitis asam oleat dibeli dari Êxodo Científica (São Paulo – SP, Brasil). Heksana bermutu kromatografi dibeli dari Sigma-Aldrich (St Louis, AS). Etanol diperoleh dari Neon (São Paulo, Brasil). Semua reagen lain yang digunakan bermutu analitis, dan dibeli dari Sigma-Aldrich atau Dinâmica (São Paulo, Brasil).
Ekstraksi lignin dari ampas jambu mete (CAB)
Pertama, 30% (b/v) ampas apel jambu mete diolah dengan 0,6 mol L −1 asam sulfat pada 121 °C selama 15 menit dalam autoklaf (Araraquara, Brasil). Kemudian, fraksi padat dipisahkan dan diolah dengan 1,0 mol L −1 natrium hidroksida pada kondisi yang sama (121 °C selama 15 menit dalam autoklaf), menurut metodologi yang dijelaskan oleh Rocha et al . 17 Fraksi cairan gelap yang dihasilkan dari perlakuan alkali dipisahkan dengan filtrasi vakum. Lignin yang ada dalam fraksi ini diendapkan dengan pengasaman menggunakan 75% (v/v) asam sulfat, mengikuti protokol yang dijelaskan oleh Serpa et al . 7 Lignin yang dihasilkan dicuci dengan air suling dan dikeringkan pada 60 °C selama 24 jam.
Sintesis nanokomposit magnetik lignin dan persiapan biokatalis
Sintesis nanopartikel magnetik lignin (Lig-MNP) dilakukan sesuai dengan metodologi yang dijelaskan oleh Serpa et al . 7 Kemudian, komposit Lig-MNP dikeringkan pada suhu 25 °C dalam desikator dan digunakan sebagai pendukung imobilisasi.
Enzim CALB diimobilisasi pada suhu 25 °C dan 150 rpm selama 24 jam menggunakan beban 5 mg protein per gram bahan pendukung, menurut metode yang dijelaskan oleh Levy et al . 18 Biokatalis kemudian dipisahkan dengan aksi magnetik dan diberi nama Lig-MNP/CALB. Aktivitasnya ditentukan mengikuti metode yang dijelaskan oleh Serpa et al . 7
Penentuan komposisi dan kemurnian asam oleat komersial
Asam oleat dari tingkat analitis dikenakan proses metilasi untuk menentukan kandungan asam lemak. Prosedur ini dilakukan untuk mengidentifikasi ester mana, selain EO yang sedang terbentuk, memastikan presisi tertinggi dalam menganalisis sampel dari proses esterifikasi. Persiapan metil ester asam lemak (FAME) dilakukan dengan menggunakan 0,33% (b/v) asam oleat yang dilarutkan dalam heksana tingkat kromatografi. Selanjutnya, larutan NaOH 0,5 mol L −1 dalam metanol tingkat analitis ditambahkan, dan campuran dipanaskan pada 70 °C selama 3 menit. Setelah pendinginan, 5 mL larutan esterifikasi yang mengandung 10 g NH₄Cl, 300 mL metanol, dan 15 mL H₂SO₄ ditambahkan. Tabung dikocok selama 30 detik, dipanaskan kembali dalam penangas air selama 5 menit, dan kemudian didinginkan lagi. Kemudian, 4 mL larutan NaCl jenuh ditambahkan, diikuti oleh 3 mL heksana kromatografi–kelas, dengan pengocokan kuat setelah setiap penambahan. Campuran tersebut kemudian dipindahkan dan supernatan dikumpulkan untuk analisis kromatografi gas-spektrometri massa (GC-MS). Prosedur ini dilakukan menurut metodologi yang dijelaskan oleh Embrapa Agroindústria Tropical, 19 Instituto Adolfo Lutz, 20 dan Asosiasi Ahli Kimia Analisis Resmi. 21
Analisis GC–MS dilakukan pada sistem Agilent GC-7890B (Agilent, Santa Clara, AS) yang dilengkapi dengan detektor MSD-5977A, menggunakan kolom HP-5MS dan helium sebagai gas pembawa (1,00 mL min −1 ). Suhu ditetapkan pada 250 °C untuk injektor, 150 °C untuk detektor, dan 280 °C untuk jalur transfer. Program suhu oven dimulai pada 35 °C, ditingkatkan pada laju 15 °C min −1 hingga 180 °C, kemudian pada 5 °C min −1 hingga 250 °C, dan dipertahankan pada suhu akhir ini selama 10 menit, menghasilkan total waktu pengoperasian 33,7 menit, seperti yang dijelaskan oleh Levy et al . 18 Identifikasi senyawa dilakukan dengan membandingkan pola fragmentasi dalam spektrum massa dengan basis data NIST versi 2.0 tahun 2012. Indeks retensi dihitung menggunakan serangkaian alkana homolog (C7–C40) dan berdasarkan metodologi dari literatur. 22 – 24
Biosintesis etil oleat (EO) dikatalisis oleh CALB bebas dan terimobilisasi
Evaluasi suhu optimal, rasio molar, dan beban katalis
Reaksi esterifikasi dilakukan dengan menggunakan asam oleat dan etanol dalam medium bebas pelarut. Reaksi dilakukan dalam pengocok orbital (Tecnal, Piracicaba, Brasil) dengan CALB atau Lig-MNP/CALB bebas, menggunakan beban biokatalis 40 mg mL −1 pada 150 RPM selama 24 jam. Rasio molar asam-alkohol yang berbeda (1:1, 1:2, dan 1:5) dan suhu (35 °C, 40 °C, dan 45 °C) dievaluasi. Reaksi kontrol dilakukan tanpa enzim dalam semua kondisi. Beban biokatalis (40, 80, dan 120 mg mL −1 ) diuji dalam kondisi suhu dan rasio molar yang dioptimalkan, dengan biokatalis menunjukkan aktivitas enzimatik sebesar 13,2 U g −1 . Untuk reaksi dengan CALB bebas, media reaksi dipanaskan hingga 100 °C selama 5 menit setelah 24 jam. Dalam reaksi dengan CALB yang diimobilisasi, biokatalis dihilangkan dengan pemisahan magnetik sebelum dipanaskan hingga 100 °C selama 5 menit. Semua percobaan dilakukan dalam rangkap tiga, dan deviasi rata-rata dan uji Tukey diterapkan dengan tingkat kepercayaan 95%. Sampel dianalisis dengan kromatografi gas seperti yang dijelaskan di tempat lain. 18 Konversi asam oleat ditentukan menggunakan Persamaan 1 , di mana A OA,0 , dan A OA masing-masing mewakili area puncak asam oleat di awal dan akhir reaksi.
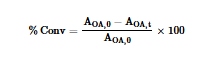
Profil kinetika produksi ester kemudian diperoleh dalam kondisi terbaik yang ditentukan menggunakan enzim bebas dan yang diimobilisasi selama 36 jam. Pada interval waktu yang telah ditentukan, sampel dari media reaksi diambil dan dianalisis dengan kromatografi gas (GC), dan konversi asam oleatnya ditentukan menggunakan Persamaan 1 .
Studi stabilitas operasional biokatalis
Dalam kondisi optimal untuk reaksi esterifikasi (dijelaskan di bagian sebelumnya), stabilitas operasional enzim dievaluasi selama lima siklus, dengan biokatalis dipisahkan secara magnetis di antara siklus. Konversi asam oleat ditentukan menggunakan prosedur yang diuraikan di bagian sebelumnya.
Pemisahan, pemurnian, dan karakterisasi etil ester
Campuran etil ester dipisahkan dengan pengendapan, dan pemurnian dilakukan dengan penguapan pada suhu 110 °C selama 2 jam sambil diaduk.
Komposisi campuran etil ester yang dimurnikan dianalisis dengan GC, menggunakan kromatografi gas Shimadzu 2010 Pro (Shimadzu, Kyoto, Jepang) dengan detektor konduktivitas termal dan detektor ionisasi nyala (GC-TCD-FID) dengan kolom Carbowax 20 M. Nitrogen digunakan sebagai gas pembawa pada laju alir 1,00 mL min −1 . Injektor dan detektor dipertahankan pada 250 °C untuk total waktu analisis 36,5 menit. Program suhu dimulai pada 50 °C, kemudian meningkat menjadi 180 °C pada 10 °C min −1 . Suhu kemudian ditingkatkan pada laju 20 °C min −1 hingga mencapai 250 °C, di mana dipertahankan selama 20 menit.
Viskositas dan densitas etil ester yang disintesis dan dimurnikan ditentukan menggunakan viskodensimeter SMV Anton Paar 3001 (Anton Paar, Graz, Austria) pada suhu 20, 40, 60, dan 80 °C. 25 Analisis data dilakukan menggunakan ANOVA dan alat uji Tukey yang tersedia di OriginPro 9.0. Tingkat signifikansi ditetapkan pada p < 0,05.
Analisis termogravimetri (TGA) diterapkan pada campuran yang dimurnikan untuk menentukan transisi fase dan dekomposisi termal biodiesel, menggunakan instrumen TGA Q500 V20.13 Build 39 (instrumen TA, New Castle, AS). Sampel dipanaskan dalam wadah platina dari 25 hingga 600 °C, dengan peningkatan pemanasan 10 °C min −1 dan laju alir N 2 50 mL min −1 . Transisi fase diperkirakan dari awal peristiwa kehilangan massa utama, yang sesuai dengan penguapan etil oleat. Kapasitas panas isobarik biodiesel ditentukan menurut metode yang dijelaskan oleh Alves et al . 26
Hasil dan Pembahasan
Pengaruh suhu, rasio molar, dan beban enzim pada sintesis etil oleat
Analisis komposisi untuk proses metilasi asam oleat komersial menunjukkan 83,2% metil oleat, 5,8% metil palmitat, 4,4% metil palmitoleat, 3,0% metil stearat, 1,8% metil miristat, 1,2% metil linoleat, dan 0,8% metil 15-metilheksadekanoat, yang merupakan asam lemak yang terdapat dalam tingkat analisis asam oleat. Nilai-nilai ini digunakan untuk menghitung konversi dalam reaksi esterifikasi.
Biokatalis yang diperoleh dari proses imobilisasi menggunakan 5 mg protein CALB per g Lig-MNP memiliki tingkat aktivitas 13,2 U/g. Biokatalis ini digunakan untuk melakukan reaksi esterifikasi dalam berbagai kondisi operasional, seperti yang ditunjukkan pada Gambar 1 .
Gambar 1
Buka di penampil gambar
Kekuatan Gambar
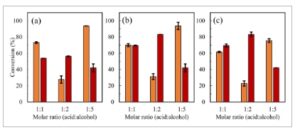
Konversi asam oleat menjadi etil oleat diperoleh pada suhu 35 °C (a), 40 °C (b), dan 45 °C (c) menggunakan CALB bebas ( ■ ) dan biokatalis Lig-MNP/CALB ( ■ ) dengan waktu reaksi 24 jam menggunakan rasio molar asam:alkohol yang berbeda.
Biokatalis Lig-MNP/CALB mencapai konversi yang melebihi 80% pada suhu tertinggi dengan rasio molar asam-alkohol 1:2. Sebaliknya, enzim bebas mencapai konversi lebih dari 90% pada suhu terendah yang dievaluasi dengan konsentrasi etanol tertinggi. Saat menggunakan rasio asam-alkohol ekuimolar, baik biokatalis maupun enzim bebas mencapai konversi yang sama pada suhu 40 °C. Namun, pada suhu 35 °C, enzim bebas mengungguli biokatalis, sedangkan pada suhu 45 °C, biokatalis mencapai konversi tertinggi.
Pada rasio molar asam-alkohol sebesar 1:1 dan 1:5, enzim bebas dan biokatalis bekerja sesuai harapan di semua suhu yang dievaluasi. Enzim bebas menunjukkan konversi yang lebih tinggi pada suhu yang lebih rendah dan pH yang mendekati netral (yaitu, dengan kandungan etanol yang lebih tinggi), yang kemungkinan besar disebabkan oleh berkurangnya risiko deaktivasi dan denaturasi. Sebaliknya, biokatalis yang diimobilisasi menunjukkan peningkatan konversi pada suhu yang lebih tinggi, yang dikaitkan dengan peningkatan energi kinetik molekuler yang meningkatkan interaksi enzim-substrat, dan imobilisasi enzim meningkatkan stabilitas termalnya. Pada rasio molar 1:2, biokatalis secara konsisten mengungguli enzim bebas pada semua suhu yang diuji. Hasil ini konsisten dengan temuan yang dilaporkan oleh Levy et al ., 18 Martínez-Ruiz et al ., 27 dan Castro et al . 28
Hasil serupa untuk produksi EO dilaporkan oleh Panchal et al ., 29 yang menggunakan rasio molar 1:12 (asam: alkohol) pada 45 °C dan 300 rpm selama 5 jam, serta oleh Martínez-Ruiz et al ., 27 yang menggunakan 1,5 g biokatalis pada suhu yang sama. Meskipun kedua penelitian mencapai konversi tinggi dalam waktu reaksi yang lebih pendek, pendekatan mereka melibatkan pengenceran yang signifikan, baik dalam etanol 29 atau dalam n -heksana, 27 yang dapat memerlukan langkah-langkah pemisahan hilir tambahan dan intensif energi. Persyaratan ini dapat membahayakan kelayakan dan efektivitas biaya proses pada skala industri.
Dalam penelitian lain, Jurmot dan Abbas 30 memperoleh konversi sebesar 55,6% menggunakan rasio molar asam:alkohol 1:3 pada suhu 70 °C selama 2 jam. Ini merupakan hasil yang menjanjikan, tetapi suhu reaksi yang tinggi dapat meningkatkan biaya operasional, yang dapat menimbulkan keterbatasan untuk aplikasi skala besar jika dibandingkan dengan kondisi yang lebih ringan yang digunakan dalam penelitian ini.
Namun, perilaku yang tidak diharapkan diamati terkait hasil konversi saat menggunakan biokatalis yang diimobilisasi pada konsentrasi alkohol tertinggi. Penurunan konversi yang signifikan pada rasio molar asam-alkohol 1:5 dapat dikaitkan dengan sifat mekanisme imobilisasi pada penyangga Lig-NPM, yang utamanya terjadi melalui penyerapan dan aktivasi antarmuka. 11 Proses imobilisasi berbasis penyerapan dapat sensitif terhadap pelarut organik polar, seperti etanol, yang dapat mengubah konformasi struktural enzim dan mengurangi aktivitas biokatalis, seperti yang dilaporkan dalam penelitian sebelumnya. 31
Membandingkan hasil yang diperoleh oleh enzim bebas dalam rasio molar 1:2 dengan rasio yang lebih tinggi, terdapat pengurangan konversi yang drastis untuk semua suhu yang dipelajari di sini. Hasil ini dapat dikaitkan dengan pembentukan produk sampingan seperti lilin, yang diamati untuk semua rasio molar yang dievaluasi, dengan jumlah yang lebih tinggi terjadi pada rasio 1:2. Produk sampingan ini menunjukkan kelarutan yang baik dalam pelarut polar dan kelarutan yang rendah dalam pelarut apolar, dengan keasaman sedang dan konsistensi seperti agar-agar. Analisis kromatografi gas menunjukkan pembentukan dimer asam oleat, mungkin karena aksi lipase B dari Candida antarctica (EC 3.1.1.3), yang dapat dikatalisis oleh tiga reaksi utama: hidrolisis , esterifikasi , dan polimerisasi .
Studi tentang produksi dimer asam masih terbatas dalam literatur. Namun, Henderson et al . 36 melaporkan pembentukannya dalam produksi lipase pankreas, dan Gebhard et al . 37 menjelaskan penggunaan dimer asam lemak C₁₈ diacidic dalam resin akrilik.
Mengingat hasil di bagian ini, rasio molar asam:alkohol 1:2 dan suhu 40 °C dipilih untuk mengevaluasi beban katalitik optimum dalam reaksi sintesis.
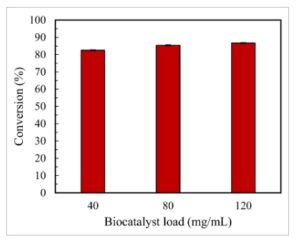
Seperti yang ditunjukkan pada Gambar 2 , beban biokatalis tidak meningkatkan konversi asam oleat menjadi EO secara signifikan. Hasil ini dapat dikaitkan dengan peningkatan kadar air, yang mungkin telah menggeser kesetimbangan reaksi reversibel ke arah reaktan, sehingga membatasi konversi. Penjelasan lain yang mungkin adalah bahwa konsentrasi enzim melebihi substrat yang tersedia, yang menyebabkan kejenuhan dan mencegah peningkatan lebih lanjut dalam konversi meskipun beban katalis lebih tinggi.
Gambar 2
Buka di penampil gambar
Kekuatan Gambar
Konversi asam oleat menjadi etil oleat diperoleh menggunakan rasio molar asam:alkohol 1:2 pada suhu 40 °C dan 24 jam dengan biokatalis Lig-MNP/CALB pada beban berbeda.
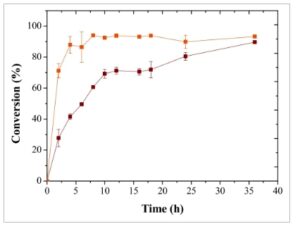
Gambar 3 menunjukkan profil konversi dari waktu ke waktu untuk reaksi esterifikasi di bawah kondisi optimum. CALB yang diimobilisasi mengubah asam oleat secara bertahap pada setiap waktu yang dievaluasi, mencapai konversi maksimum mendekati 90% pada 36 jam. Hasil serupa diperoleh oleh Gebhard et al . 37 menggunakan lipase yang diimobilisasi dalam cairan ionik polimer, dengan rasio molar 1:12 asam:alkohol pada 45 °C dan 300 rpm selama 5 jam. Panchal et al . 29 memperoleh konversi 55,6% dalam reaksi yang dilakukan pada 70 °C selama 2 jam menggunakan rasio asam:alkohol 1:3 dan zeolit 13X sebagai katalis heterogen untuk memperoleh EO. Di sisi lain, CALB bebas menunjukkan konversi mendekati 80% pada jam reaksi kedua, mencapai maksimum mendekati 95% selama 8 jam, menunjukkan sedikit deviasi standar pada jam-jam berikutnya.
Gambar 3
Buka di penampil gambar
Kekuatan Gambar
Konversi asam oleat menjadi EO dalam reaksi yang dikatalisis oleh CALB bebas ( ■ ) dan terimobilisasi ( ■ ) pada suhu 40 °C dan 150 rpm menggunakan rasio molar asam:alkohol 1:2.
Stabilitas operasional biokatalis
Gambar 4 menunjukkan konversi yang dicapai untuk berbagai siklus. Konversi dari asam oleat menjadi etil oleat menurun di seluruh siklus, bahkan di bawah kondisi optimal yang ditetapkan dalam evaluasi sebelumnya. Antara siklus kedua dan kelima terdapat penurunan konversi sebesar 8%, yang menunjukkan hilangnya aktivitas biokatalitik minimal, yang dapat dikaitkan dengan adhesi reaktan ke permukaan biokatalis, yang meningkatkan resistensi perpindahan massa di situs aktif enzim.

Gambar 4
Buka di penampil gambar
Kekuatan Gambar
Konversi asam oleat menjadi etil oleat diperoleh selama berbagai siklus reaksi yang dikatalisis oleh Lig-MNPs_CALB. Kondisi reaksi: rasio molar 1:2 (asam: alkohol), 40 °C, 150 rpm selama 24 jam setiap siklus. Huruf yang berbeda mewakili nilai dengan perbedaan yang signifikan (tingkat kepercayaan 95%).
Penurunan konversi ini juga dapat dikaitkan dengan desorpsi enzim, yang dapat terjadi karena air yang dihasilkan selama reaksi. Keberadaan air dapat mengganggu gaya van der Waals yang bertanggung jawab untuk mempertahankan perlekatan CALB ke Lig-NPM, yang menyebabkan pelindian enzim parsial. Fenomena ini telah dilaporkan sebelumnya oleh Pulido et al . 31 Meskipun demikian, biokatalis mempertahankan kemampuannya untuk mengkatalisis konversi asam oleat menjadi etil oleat karena proses imobilisasi melibatkan tiga mekanisme berbeda: penyerapan, aktivasi antarmuka, dan pengikatan kovalen. 11
Karakterisasi etil ester murni
Campuran etil ester yang dimurnikan terutama terdiri dari etil oleat (88,01 ± 0,04%), dengan jumlah etil stearat yang lebih kecil (5,05 ± 0,13%), etil palmitat (3,85 ± 0,06%), etil linoleat (1,66 ± 0,04%), dan etil palmitoleat (1,43 ± 0,06%).
Gambar 5(a) menunjukkan media reaksi yang dikatalisis dengan Lig-MNP/CALB dalam warna yang lebih gelap daripada yang diperoleh menggunakan CALB bebas. Perbedaan ini dapat dikaitkan dengan keberadaan lignin dalam media reaksi. Namun, biodiesel potensial tetap berupa larutan bening, terutama setelah pemurnian. Gambar 5(b) menunjukkan esterifikasi asam oleat dalam etanol menggunakan produk sampingan CALB bebas. Pembentukan dua fase yang tidak bercampur dapat diamati, salah satunya bersifat apolar dan kaya akan EO, dan yang lainnya tampak polar dan mungkin kaya akan dimer asam oleat, seperti yang dibahas sebelumnya.

Gambar 5
Buka di penampil gambar
Kekuatan Gambar
Etil ester diproduksi menggunakan rasio molar asam:alkohol 1:2 pada suhu 40 °C yang dikatalisis oleh CALB yang diimobilisasi (Lig-MNP/CALB) (a), dan oleh CALB bebas (b) dan (c) EO murni yang diperoleh menggunakan Lig-MNP/CALB.
EO yang diperoleh dalam reaksi yang dikatalisis menggunakan CALB yang diimobilisasi juga menunjukkan homogenitas, kejernihan, dan tidak adanya pengotor yang terlihat, seperti yang terlihat pada Gambar 5(c) . Karakteristik ini sejalan dengan Resolusi 920, 38 Agência Nacional do Petróleo, Gás Natural e Biocombustíveis (ANP) yang menetapkan spesifikasi untuk biodiesel di Brasil.
Tabel 1 menunjukkan massa jenis etil ester murni, viskositas dinamis, dan kapasitas panas. Seperti yang diharapkan untuk cairan biasa, massa jenis dan viskositas menurun seiring dengan suhu.
Tabel 1. Sifat fisikokimia (massa jenis, viskositas kinematik, dan kapasitas panas) etil ester murni yang dievaluasi pada suhu yang berbeda.
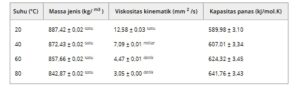
Catatan: Huruf superskrip yang identik dalam kolom menunjukkan tidak ada perbedaan yang signifikan secara statistik antara nilai properti yang bersesuaian.
Massa jenis etil oleat pada suhu 20 °C berada dalam kisaran yang ditetapkan untuk biodiesel (850 hingga 900 kg m −3 ) oleh Agência Nacional do Petróleo (ANP) 38 . Akan tetapi, viskositas kinematik etil oleat pada suhu 40 °C adalah 42% di atas kisaran viskositas (3 hingga 5 mm 2 s −1 ) yang ditetapkan dalam resolusi ANP 38 yang menetapkan sifat-sifat biodiesel. Akan tetapi, etil oleat dilaporkan memiliki viskositas 4,73 mm 2 s −1 pada suhu 40 °C dan 0,1 MPa. 39
Kapasitas kalor isobarik (CP) biodiesel meningkat seiring dengan suhu, seperti yang diharapkan untuk cairan. Pada suhu 20 °C, CP adalah 589,98 ± 3,10 kJ mol −1 K −1 , meningkat secara bertahap menjadi 641,76 ± 3,43 kJ mol −1 K −1 pada suhu 80 °C. Tren ini menunjukkan bahwa lebih banyak energi diperlukan untuk menaikkan suhu seiring dengan peningkatan energi kinetik molekul, yang pada gilirannya memerlukan masukan energi tambahan untuk mempercepat pergerakannya lebih jauh.
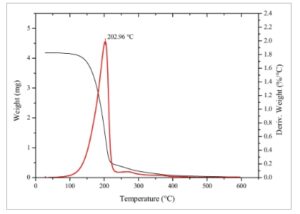
Gambar 6 menunjukkan profil termogravimetrik dari EO yang dimurnikan selama proses pemanasan. Kehilangan massa yang nyata dimulai pada sekitar 203 °C, yang menunjukkan transisi fase dari cair menjadi uap. Kehilangan massa total mencapai 99,8% pada 600 °C, yang menunjukkan bahwa sampel tersebut hampir seluruhnya terdiri dari komponen yang mudah menguap, dengan hanya sedikit pengotor yang tidak mudah menguap atau stabil secara termal yang tersisa. Hasil ini menunjukkan kemurnian tinggi dari EO yang disintesis.
Gambar 6
Buka di penampil gambar
Kekuatan Gambar
Analisis termogravimetri (TGA) dari EO murni, menunjukkan berat total (■) dan turunan berat terhadap suhu ( ■ ).
Kesimpulan
Sintesis ester oleat, yang memiliki berbagai aplikasi industri, dicapai dengan menggunakan CALB yang diimobilisasi pada media berbiaya rendah yang terdiri dari magnetit dan lignin yang diekstraksi dari CAB, produk sampingan agroindustri. Sintesis etil ester mencapai konversi sekitar 90% dengan beban katalitik 40 mg biokatalis per mL media reaksi pada suhu 40 °C dan 150 rpm, menggunakan rasio molar asam:alkohol 1:2 selama periode 36 jam. Lig-MNP/CALB dapat digunakan kembali untuk reaksi selanjutnya. Etil ester yang dimurnikan menghasilkan kandidat biodiesel dengan kemurnian ester total 98%. Karakteristik dan sifat fisik dan kimia dianalisis, mengonfirmasi potensi ester untuk aplikasi yang dimaksudkan dan kepatuhan terhadap undang-undang yang relevan. Pendekatan ini menghasilkan senyawa, termasuk biodiesel, dengan dampak lingkungan yang lebih rendah, mendukung proses berkelanjutan dan pengembangan ekonomi yang kurang berpolusi.

